




|
Les filtres respiratoires offrent une barrière efficace prévenant la contamination croisée entre les patients, les circuits respiratoires, les équipements de ventilation et d'anesthésie, et l'environnement clinique. Leur utilisation est aujourd'hui largement reconnue comme bénéfique et est recommandée par de nombreuses Associations d'Anesthésistes(1). Ils sont largement utilisés partout dans l'hopital, notamment au bloc opératoire, en soins intensifs, en exploration fonctionnelle respiratoire et en unité de soin respiratoire.
Les Echangeurs de Chaleur et d'Humidité (ECH) minimisent la perte par les gaz expirés du patient, et, combinés à un média filtrant (Filtre Echangeur de Chaleur et d'Humidité, FECH), ils réduisent également le risque de contamination croisée dans l'environnement clinique. |
||||||||

|
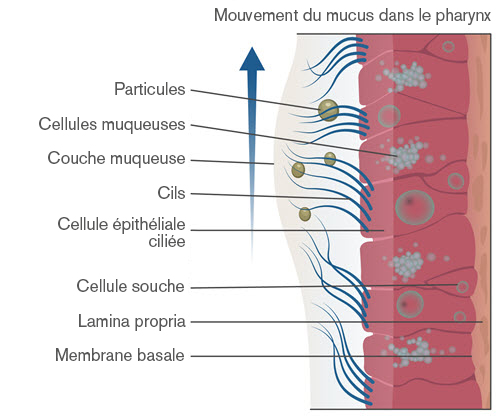
La fonction normale des voies aériennes supérieures du corps est de filtrer, humidifier et réchauffer l'air que nous inspirons. L'air est réchauffé en traversant un vaste réseau de capillaires dans le nez. Les membranes muqueuses tapissent les voies aériennes supérieures et aident à humidifier l'air et à piéger les particules aéroportées (poussières et microbes). Les cils mobilisent le mucus hors des poumons et en direction du pharynx pour être évacué. Les voies aériennes supérieures aident également à conserver la chaleur et l'humidité qui seraient normalement perdues lors de la phase expiratoire. Les gaz quittant les poumons pendant l'expiration sont à la température corporelle (37°C), ont une Humidité Absolue (HA) de 44mg/l H2O et une Humidité Relative (HR) de 100%. Lorsque un patient expire, la chaleur et l'humidité sont retenues par les voies aériennes supérieures puis restituées aux gaz inspirés suivants, qui sont normalement plus froids et secs selon les conditions ambiantes. La large surface des voies aériennes supérieures est particulièrement efficace. Elle aide à minimiser tout effet secondaire potentiel associé à l'inhalation de gaz froids et secs sur une période prolongée. Cette protection physiologique naturelle est contournée quand une prothèse ventilatoire est introduite, par exemple un tube trachéal, un dispositif supraglottique ou un tube de trachéotomie. Le gaz-source dispose alors d'un accès direct aux poumons, organe sensible et fragile, et ceci peut entrainer de fait une augmentation du risque potentiel d'infection et de contamination croisée microbienne. Ceci peut également entrainer un refroidissement et un assèchement des voies aériennes résultant de l'inspiration de gaz médicaux frois et secs sur une période prolongée. Normalement, l'air ambiant intérieur est approximativement à 23°C avec une HR de 60% et une HA de 21mg/l. Les gaz médicaux sont typiquement entre 10 et 15°C avec une HR de 0 à 2 % et une HA de 0.5 mg/l, ce qui peut davantage accroitre le risque. Ceci peut conduire à la détérioration des cils, l'épaississement du mucus, la formation de croutes muqueuses responsables d'une augmentation du risque d'occlusion du tube, l'accroissement du risque d'infection, l'atélectasie et l'accroissement des coûts en raison de la prolongation du séjour à l'hopital. |
 |
|||||||
Infection Protection du patient Les patients gravement malades avec une immunité réduite sont typiquement plus exposés au risque d'infections. Ces infections nosocomiales entrainent l'augmentation potentielle des morbidités et de la mortalité et ont un impact significatif sur le coût des soins du patient du fait de la prolongation du séjour à l'hopital. L'utilisation stratégique d'un filtre respiratoire performant et dûment validé offre une barrière efficace entre le patient, le circuit respiratoire et l'équipement, afin de réduire le risque de contamination croisée. |
Contamination croisée Protection du circuit respiratoire La protection physiologique naturelle est contournée chez les patients nécessitant l'introduction d'une prothèse ventilatoire artificielle. Ceci augmente le risque d'infection et de contamination croisée entre les patients et l'équipement de soins. La contamination croisée des patients, via le circuit d'anesthésie, a fait l'objet de rapports et est très bien documentée(2). Les préoccupations concernant les infections incluent notamment l'Hépatite C, la Tuberculose, les projections de sang, le SRAS et autres coronavirus similaires. |
Protection de l'équipement respiratoire et de l'environnement clinique Protection de l'équipement L'utilisation de filtres respiratoires performants et adaptés peut offrir une protection des appareils fragiles et couteux, pour aider à préserver leurs fonctionnalités, réduire les frais d'entretien et prévenir le risque potentiel de contamination croisée. |
||||||

| Le seul moyen pour un clinicien de déterminer les performances et l'efficacité d'un filtre respiratoire, d'un ECH et d'un FECH est d'avoir de plus en plus recours à des protocoles de test normalisés. Il est essentiel de s'assurer que les données sont cliniquement pertinentes, à jour et reflètent le dispositif que le clinicien utilise. Nos gammes de filtres respiratoires et de FECH ont été testées en toute indépendance et ont prouvé leurs hautes efficacités dans la prévention du passage de bactéries et virus. Ces tests fournissent des informations cliniquement pertinentes permettant de choisir, selon les preuves recueillies, le dispositif le plus adaptés aux exigences cliniques. Tests microbiologiques Tous nos filtres sont testés en laboratoires spécialisés en microbiologie, contre les attaques de bactéries et virus cliniquement pertinents. Ceci est normalement réalisé grâce au développement de protocoles spécifiques simulant les types d'attaques qu'un filtre peut subir dans un environnement clinique. Une particule spécifique est choisie pour simuler la taille des bactéries et virus communément rencontrés. Chaque filtre et FECH individuel d'Intersurgical est testé et ses performances vérifiées en ce sens. Ces tests cliniquement adaptés sont réalisés sur tous nos produits avec Bacillus subtilis (1.0μm x 0.7μm) et Ø174 bactériophage (0.027μm). Ces tests fournissent des informations cliniquement pertinentes permettant de choisir, selon les preuves recueillies, le dispositif le plus adaptés aux exigences cliniques, et d'attester de son efficacité avec d'autres organismes de taille pertinente fréquemment rencontrés dans l'environnement clinique.  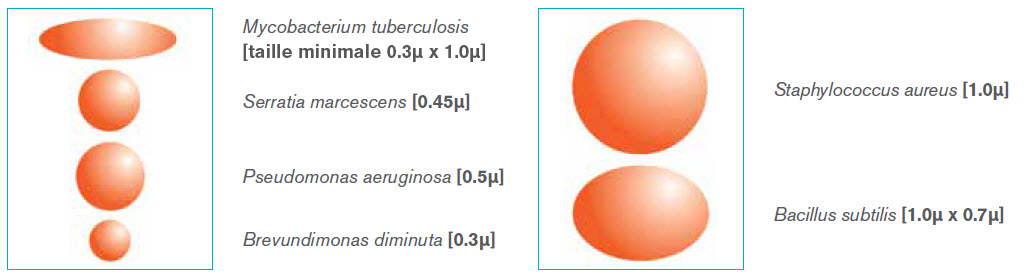 Le taux de passage des organismes détermine l'efficacité du filtre. Cette efficacité est exprimée en pourcentage, basé sur le nombre initial d'organismes attaquant le filtre par rapport au nombre d'organismes le traversant. 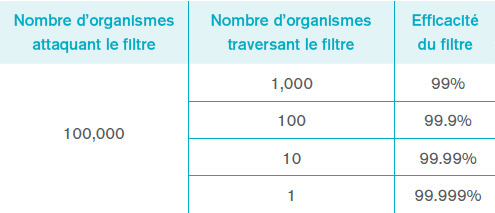 L'attaque présentée dans le protocole de test viral (φ174 bactériophage, 0.027 μm) sera à minima aussi sévère que celle posée par le Coronavirus (COVID-19). Les attestations de performance sont disponibles sur demande pour chaque produit individuel. 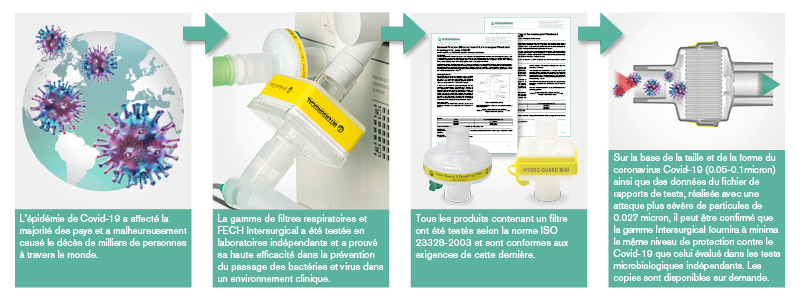 |
|||||||||